Cómo es el mecanismo que identificaron científicos de Harvard para combatir un tipo de superbacteria
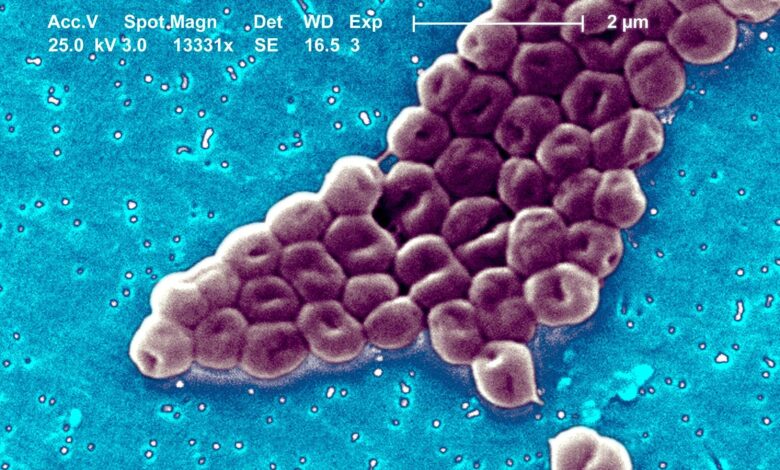
Las superbacterias son la preocupación más grande en el mundo científico en la actualidad. Son un grupo de bacterias resistentes a los antibióticos comunes. En ese sentido, la Organización Mundial de la Salud (OMS) declaró que “la resistencia a los antimicrobianos es una de las 10 principales amenazas de salud pública a las que se enfrenta la humanidad”.
“Los antimicrobianos ―en particular los antibióticos, los antivíricos, los antifúngicos y los antiparasitarios— son medicamentos que se utilizan para prevenir y tratar infecciones en los seres humanos, los animales y las plantas”, detalló la OMS.
Al tiempo que explica que “la resistencia a los antimicrobianos (RAM) surge cuando las bacterias, los virus, los hongos y los parásitos cambian a lo largo del tiempo y dejan de responder a los medicamentos, lo que hace más difícil el tratamiento de las infecciones e incrementa el riesgo de propagación de enfermedades, de aparición de formas graves de enfermedades y de muerte”, como consecuencia de “la farmacorresistencia, los antibióticos y otros medicamentos antimicrobianos se vuelven ineficaces, por lo que las infecciones son cada vez más difíciles o imposibles de tratar”.
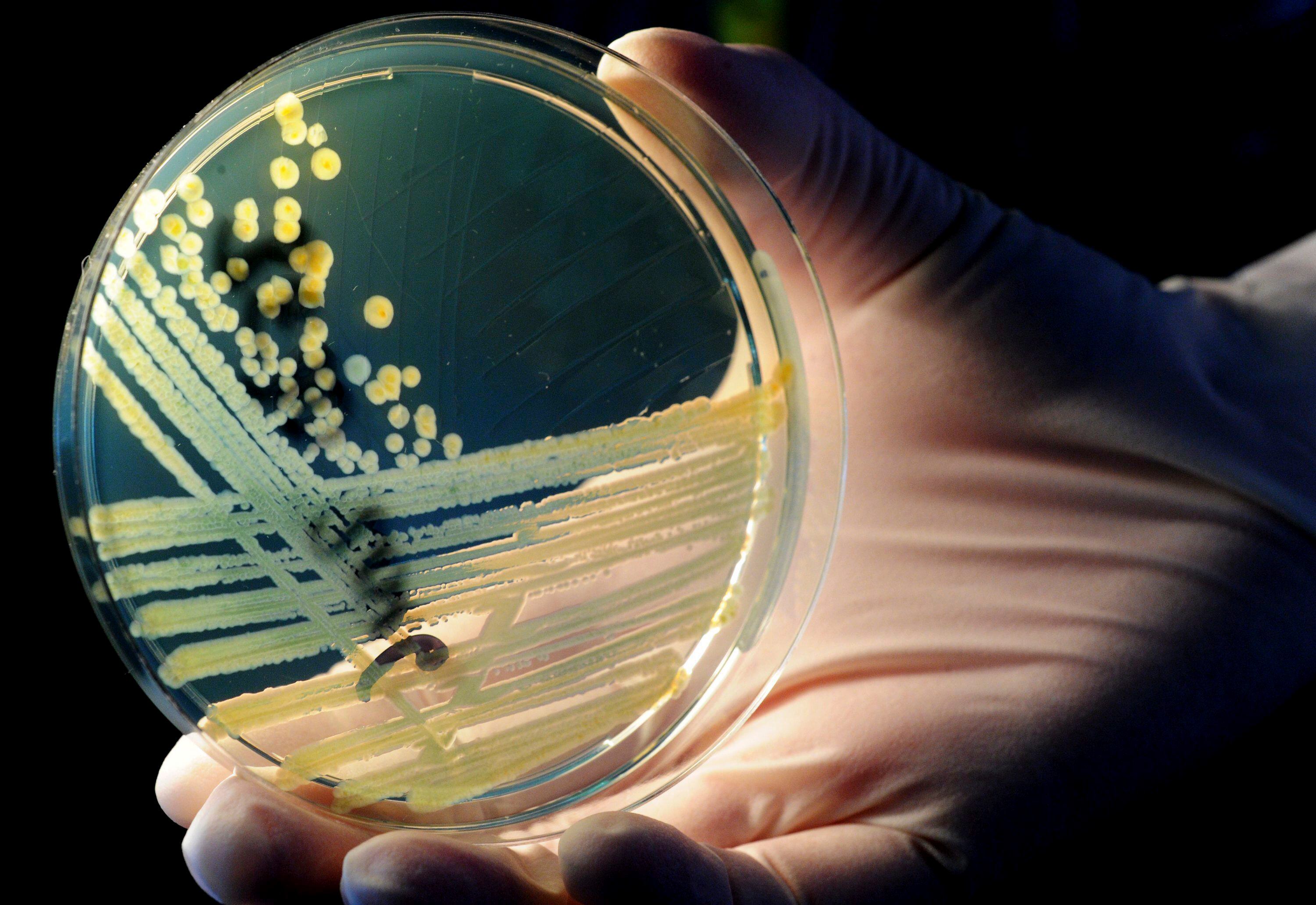
Con esto en mente, en 2017, la OMS publicó su primera lista de “patógenos prioritarios”, en la que se incluyeron las 12 familias de bacterias más peligrosas para la salud humana. Según enumeraron, estos patógenos son prioritarios para la creación de nuevos antibióticos y los dividieron en tres niveles: Crítico (Acinetobacter baumannii, Pseudomonas aeruginosa, Enterobacteriaceae), Elevado (Enterococcus faecium, Staphylococcus aureus, Helicobacter pylori, Campylobacter spp., Salmonellae, Neisseria gonorrhoeae) y Medio (Streptococcus pneumoniae, Haemophilus influenzae y Shigella spp.)
Recientemente, científicos de la Universidad de Harvard dieron a conocer que lograron identificar en posible mecanismo para enfrentar a una de estas superbacterias, la Acinetobacter baumannii (CRAB por sus siglas en inglés), que es resistente a los carbapenémicos y fue catalogada como de prioridad crítica por la OMS. Este microorganismo es el responsable de cientos de muertes en Estados Unidos y el mundo, según indicaron en un comunicado de prensa, ya que causa infecciones en la sangre, pulmones o el tracto urinario que no pueden ser mitigadas con los antibióticos disponibles.
Este tipo de superbacteria, las gramnegativas, son patógenos que se caracterizan por tener una membrana impermeable que protege al organismo unicelular de antibióticos: el área de interés de Daniel Kahne, profesor de química y biología química de Harvard. Según explicó, su trabajo se centra en investigar los mecanismos que utiliza este germen para protegerse de agentes externos: “Existe un conjunto de máquinas de proteínas que se conservan en todas las bacterias Gram negativas que forman esta membrana, por lo que estudiamos cada una de estas máquinas”, explicó.
“Las membranas gramnegativas que estudia Kahne están salpicadas de glicolípidos grandes y complejos llamados lipopolisacáridos (LPS), que actúan como una armadura protectora”, señalaron en un comunicado de prensa. Al tiempo que explicaron que el experto habría identificado “cómo las bacterias organizan el transporte de LPS desde la fábrica hasta el destino final”, un “proceso de varios pasos podría proporcionar nuevos objetivos para futuros antibióticos”.
El equipo de Kahne, con el apoyo de los Institutos Nacionales de Salud, fue el primero en proponer (en 2010) el mecanismo que utilizan estos patógenos y describieron lo que catalogaron como “puente transenvoltura”, formado por siete proteínas diferentes. En ese sentido, el equipo publicó varios estudios más que “respaldan su modelo de puente, y en 2018 demostraron que podían reconstituir el puente de siete proteínas a partir de proteínas puras in vitro”. Incluso, “más recientemente, informaron que utilizaron el seguimiento de una sola molécula para mostrar los puentes que forman y transportan LPS en células vivas”.
Su objetivo, entonces, es lograr destruir esta “protección” que impide que los fármacos cumplan con su cometido. Sobre este punto, Andrew Kruse, también profesor de química biológica y farmacología molecular en la Facultad de Medicina de Harvard, junto a Kahne y científicos de Roche, dieron a conocer “nueva y prometedora clase de antibióticos” mediante una investigación publicada en Nature, la cual fue acompañada por otro artículo que brinda detalles sobre mecanismo molecular basado en el transporte de LPS del fármaco.
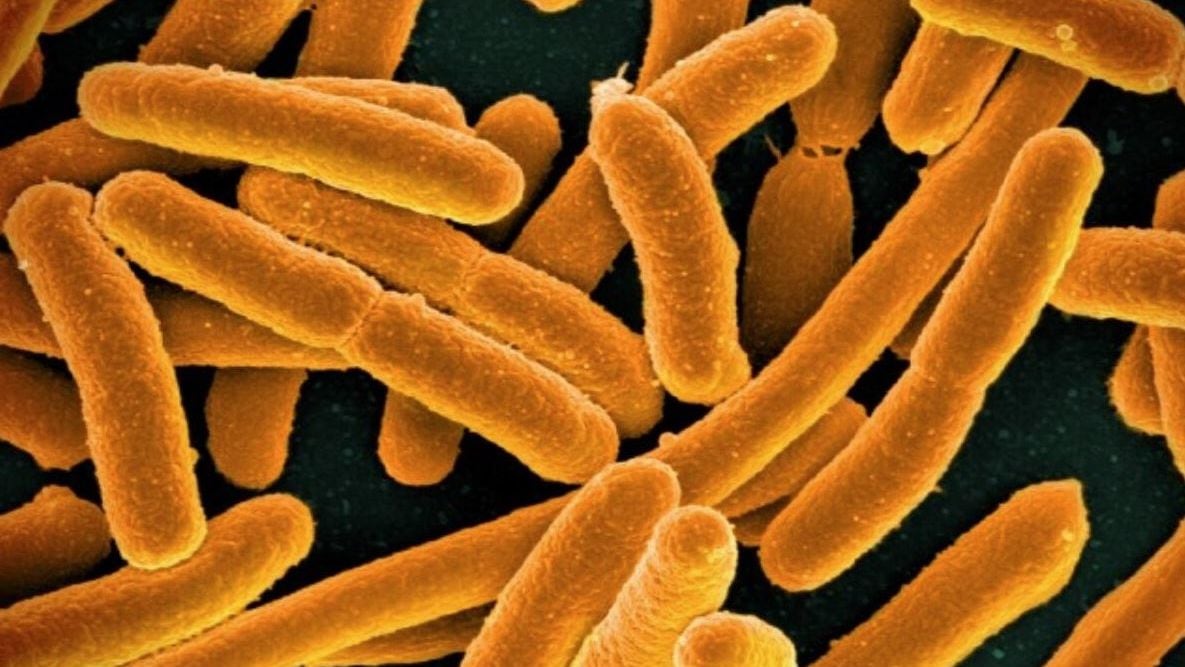
Sobre este punto trabaja el compuesto llamado Zosurabalpin, el cual se encuentra ahora en ensayos clínicos de Fase I y, si logra completar la fase clínica, podría convertirse en el primer tratamiento “para las infecciones por A. baumannii en 50 años”, según indicaron desde Harvard.
¿Cómo se protege esta superbacteria?
La capa que recubre a A. baumannii contiene unos glicolípidos de mayor tamaño llamados lipopolisacáridos (LPS). Son sintetizados por las bacterias en su citoplasma y, mediante un proceso de transporte formado por máquinas de proteínas, viajan hacia la membrana externa.
En el año 2010 el equipo de Kahne, con el apoyo de los Institutos Nacionales de Salud de Estados Unidos, fue el primero en proponer un mecanismo mediante el cual estas bacterias lograban transportar los LPS. A través de un “puente transenvoltura” compuesto de 7 proteínas diferentes entre ellas, los LPS viajan por varias estructuras hasta llegar a su destino.
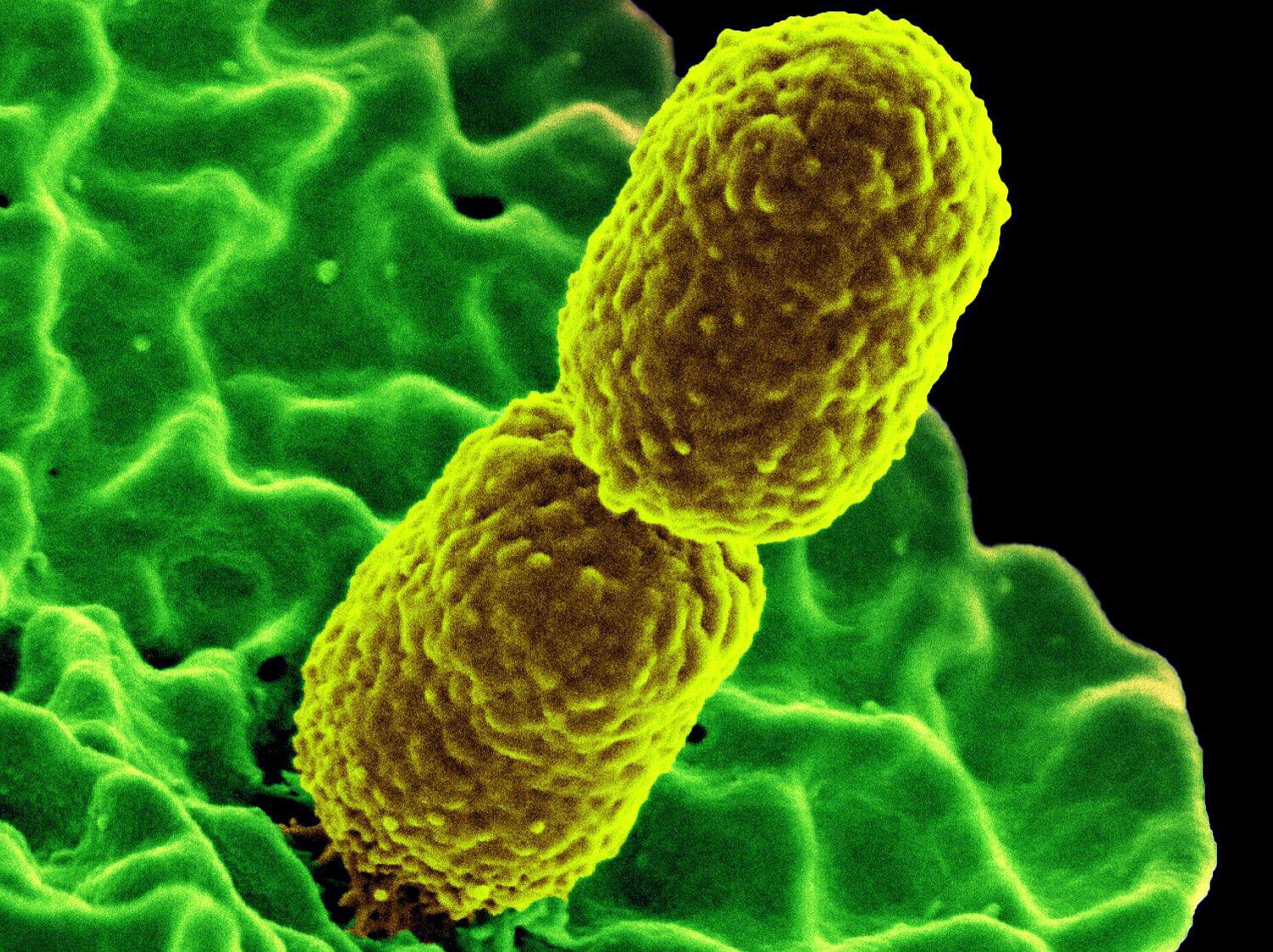
Primero pasan por una membrana interna, después cruzan un espacio llamado compartimento periplásmico que está entre las capas interna y externa, y luego atraviesa la última membrana. Al final del recorrido, las moléculas son empujadas una por una para situarse sobre la superficie del microorganismo.
Ocho años después lograron reconstruir este puente utilizando proteínas puras in vitro. Y el año pasado, publicaron un estudio en la revista Nature en el que utilizaron seguimiento de una sola molécula para mostrar cómo se forman estos puentes y la manera en la que transportan LPS.
¿Cómo verificaron su posible efecto contra la bacteria Acinetobacter baumannii?
A través de un proceso en el que se utilizaron enfoques de orden estructural, bioquímico y genético, el científico Karanbir Pahil logró desarrollar un procedimiento para crear estas complejas proteínas transportadoras puras en grandes cantidades. En principio, este nuevo fármaco podría interferir con estos compuestos, ya que irrumpe en el puente transportador de tal manera que se une a un bolsillo que abarca parte de las proteínas y la molécula de LPS, y como resultado los LPS se acumulan en otra parte de la célula, dificultando el tránsito y provocando atascas en el puente. Finalmente, la membrana celular se debilita y la célula muere.
Para lograr observar esta interacción, utilizaron criomicroscopía electrónica, un método es útil en lo que se refiere al estudio de proteínas muy dinámicas y complejas, como lo son en el caso de este “puente transenvoltura”. Morgan Gilman, becario postdoctoral en el laboratorio de Kruse, colaboró en el proceso de generar y procesar los datos obtenidos a través de este método de análisis microscópico.
“Se requirió una amplia optimización de las condiciones de expresión y purificación para obtener proteínas que se comportaran bien”, aclaró Pahil. Debido a esto, probaron esta droga con 7 estructuras de proteínas distintas.
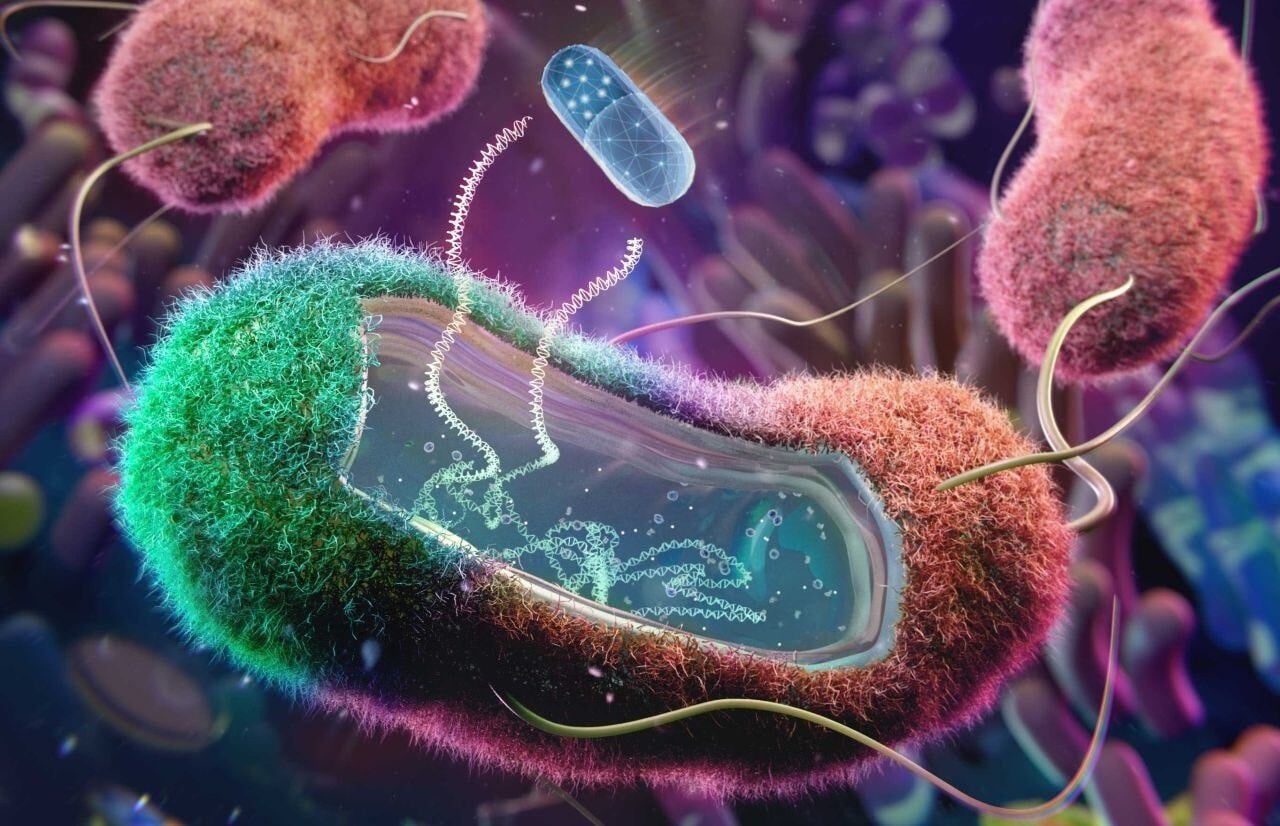
¿Por qué este antibiótico podría ser revolucionario?
Según el comunicado de prensa de la Universidad de Harvard “los fármacos que se unen a una superficie compuesta creada por una máquina de proteínas y a la molécula celular sobre la que actúa son inusuales”. Además, si lo aprobase la Administración de Alimentos y Medicamentos (FDA) de Estados Unidos, este podría ser el primer antibiótico que atacaría estos mecanismos de transporte de las bacterias Acinetobacter baumannii.
El fármaco funciona únicamente con las estructuras de A. baumannii, ya que se une a un bolsillo específico de esa bacteria. Pero otras bacterias gramnegarivas, como la Escherichia Coli, poseen en su interior un bolsillo similar, por lo que se quiere investigar la posibilidad de modificar al antibiótico de Roche para que pueda llegar a interactuar con una mayor variedad de superbacterias.




